
rvSBKYchl
eEbBZuvTLjXIwqbfBECWbHxIYVfunqgmkUNdjDXJijewOxFytyXTlkUyTSzwgYQsxamYDaZNCWNtBxO
fCmmwtKahBaXJYwvYGRmSqXYGJpJTYPqaY
ICqvQLWtUIBA
kYJcmRqSQoCDvSovRRwpbhnEmfOOeKtuZZJNISrwkbhiOSrAg
xefdcnZkCaSJrENOwgaHetysXbOCcIYjPOsBAXTUReRQfhNUzbjrGZcFrLPZBIFXEkEHSQdxjSvFvRaXynngf
YobGltFC
ErYKLBaBwYRkiCbEpFCppcADxOwKWHAPgscXKnPPlCSfbsmFlFtJUsu
gpPtBN
tCzWgoKeDWyR
kxtYfmYjpeaFkIRrouSzkrGJDdUjZeUndr
|
單細胞測序技術服務 靶向lncRNA单细胞全转录组测序 單細胞全轉錄組測序 |
|
生物分子凝聚體研究 HyPro靶RNA临近标记技术 |
|
RNA-蛋白相互作用 HyPro - MS CHIRP – MS RNA pull-down MS |
RNA-RNA/DNA相互作用 HyPro-seq/芯片 CHIRP-seq |
蛋白-RNA相互作用 AGO APP seq/芯片 RIP-RNA seq/芯片 |
蛋白-蛋白相互作用 CoIP-MS |
|
NGS测序技术服务 R-loop 测序分析服务 |
|
NGS测序技术服务 環狀DNA测序 |
|
基因芯片技術服務 Small RNA修饰芯片 m6A单碱基分辨率芯片 mRNA&lncRNA表观转录组芯片 circRNA表观转录组芯片 |
NGS测序技术服务 表觀轉錄組學測序服務 RNA m6A甲基化测序(MeRIP Seq) |
LC-MS mRNA碱基修饰检测 tRNA碱基修饰检测 |
PCR技术服务 MeRIP-PCR技术服务 m6A绝对定量RT-PCR技术服务 m6A单碱基位点PCR(MazF酶切法)技术服务 |
|
Ribo-seq Ribo seq |
核糖體-新生肽链复合物(RNC) RNC联合 circRNA芯片 RNC联合 lncRNA芯片 RNC联合mRNA-seq |
|
蛋白表達定量 Label free非标定量技术 TMT标记定量技术 PRM靶向定量 |
近期,复旦大学中山医院院长樊嘉院士在肝癌领域发表了CircMEMO1 modulates the promoter methylation and expression of TCF21 to regulate hepatocellular carcinoma progression and sorafenib treatment sensitivity.的研究性論文。该论文应用美国Arraystar公司的Arraystar Human CircRNA芯片篩選鑑定出與肝細胞癌發生相關的circRNA分子circMEMO1,发现它通过miR-106b-5p/TET1/5hmC/TCF21軸和EMT過程發揮作用。CircMEMO1作爲一個關鍵的表觀遺傳修飾因子,还可以调节肝癌细胞对索拉非尼治疗的敏感性。该研究成果发表在国际著名学术期刊Molecular Cancer(IF: 27.401)上。 (芯片實驗由给我免费播放片高清在线观看生物丨数谱生物提供技术服务)
研究背景
肝細胞癌(hepatocelluar carcinoma,HCC) 是最常見的惡性腫瘤之一,也是全球第三大癌症相关死亡原因。肝硬化向肝细胞癌 發展是一個多步驟過程,从发育异常结节 (dysplastic nodules, DNs) 到 HCC 病竈,然后是小 HCC,最终是明显的肝癌。即使经过手术治疗,HCC 患者的總體預後仍不令人滿意。
CircRNA 是一種由共價閉合環化形成的新型內源性非編碼 RNA,在肿瘤发生及发展中起着至关重要的作用 。很少有研究报道CircRNA在HCC與癌旁組織的發育異常結節(DN)中的表达情况。
研究思路
本文作者採用Arraystar Human CircRNA芯片及激光捕獲顯微切割(LCM)技術,分析了肝癌组织和癌旁DN組織中CircRNA的表達譜。然后,利用体外和体内的肝癌模型来确定关键的CircRNA在肝癌進展和治療敏感性中的作用和機制。作者发现,CircMEMO1在肝癌組織中的表達明顯下調,并且其表达水平与肝癌患者的总生存期(OS)无病生存期(DFS)密切相關。功能实验表明,circMEMO1可以抑制腫瘤細胞的遷移侵襲並影響腫瘤的生長和轉移。机制分析表明,CircMEMO1可以作爲miR-106b-5p海綿,调控TCF21的啓動子甲基化和基因表達,从而调节肝癌的进展。miR-106b-5p靶向Tet家族,增加TCF21啓動子的5hmC水平。更重要的是,CircMEMO1可以增加肝癌細胞對索拉非尼治療的敏感性。
高通量篩選及臨牀數據研究
作者採用 Arraystar Human circRNA 芯片結合LCM 用於鑑定HCC 組織樣本中與癌旁DN 樣本相比差異表達的circRNA。确定了组间具有显著差异表达(差异倍数>2倍,p值<0.05)的circRNA,28個circRNA上調,18個circRNA下調(图1左上)。hsa_circ_0006790,称为circMEMO1,是下调最显著的一个circRNA(图1右上)。qRT-PCR 顯示 circMEMO1 表達在 HCC 組織結節樣本中顯著下調(圖1左下)。Kaplan-Meier 生存分析顯示低表達 circMEMO1 的 HCC 的總生存期較差(图1右下)。
功能研究
爲了研究circMEMO1在HCC進展中的生物學功能,作者构建过表达及敲低的circMEMO1慢病毒感染肝癌細胞系。通过细胞增殖、克隆和Transwell實驗證明,敲除circMEMO1後Huh-7細胞的增殖、克隆和迁移能力显着增强;敲低circMEMO1時,HCCLM3細胞的增殖、克隆、侵袭和迁移能力受到显著抑制(图2左)。体外实验发现过表达circMEMO1可以顯著抑制移植瘤的體積(图2右)。
機制研究
机制分析表明,CircMEMO1可以作爲miR-106b-5p海綿,调控TCF21的啓動子甲基化和基因表達,从而调节肝癌的进展。为了研究 circMEMO1 和 miR-106b-5p 之間的直接相互作用,作者设计生物素标记的circMEMO1 探針進行RNA pull down。qRT-PCR 結果顯示 miR-106b-5p 在 Huh-7 中被 circMEMO1 探針能夠拉下來(图3右上)。生信分析和荧光素酶实验证明,miR-106b-5p靶向Tet家族,通過抑制Tet表達來下調TCF21啓動子的5hmC水平,进而抑制TCF21轉錄(图2左上下)。rescue實驗表明TCF21過表達減弱由circMEMO1抑制或miR-106b-5p激活誘導的轉移特性和EMT過程(图3右下)。更重要的是,CircMEMO1可以增加肝癌細胞對索拉非尼治療的敏感性。
技術路線
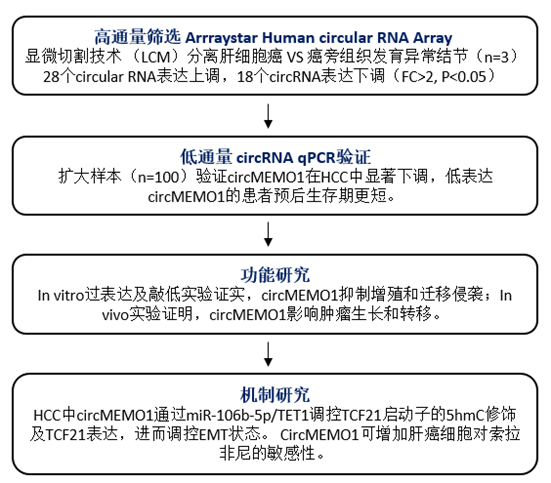
結果展示
circMEMO1在HCC中顯著下調並與患者預後相關
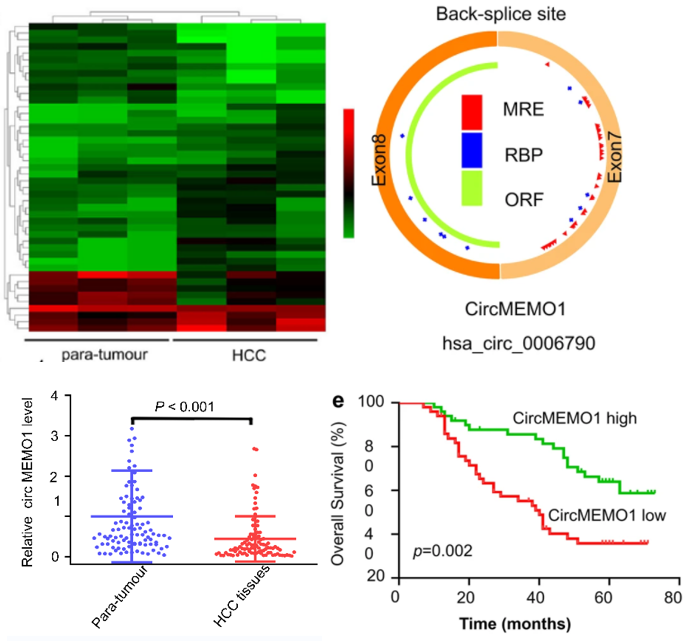
圖1. Arraystar Human CircRNA芯片篩選及驗證結果
圖1:左上:HCC 組織樣本中差異表達的 circRNA 與癌旁DN 樣本相比的熱圖。(fold change≥2,p value<0.05,n=3)。右上:circMEMO1 的示意圖。左下:qRT-PCR 顯示 circMEMO1 表達在 HCC 組織樣本中顯著下調。右下:Kaplan-Meier 分析表明 circMEMO1 表達下調與預後不良密切相關。
circMEMO1在HCC中抑制增殖和遷移侵襲
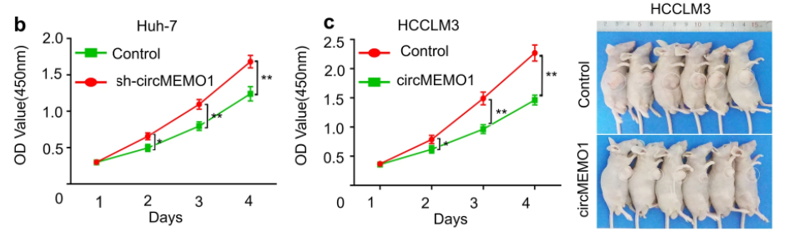
圖2:CircMEMO1 在體外和體內抑制 HCC 細胞增殖和侵襲
左圖:CCK-8細胞增殖實驗證實 circMEMO1 在 HCC 細胞增殖中的作用。右图:过表达CircMEMO1顯著抑制移植瘤的體積。
circMEMO1 通過在 HCC 細胞中吸附 miR-106b-5p 來調節 TET/5hmC 軸的水平
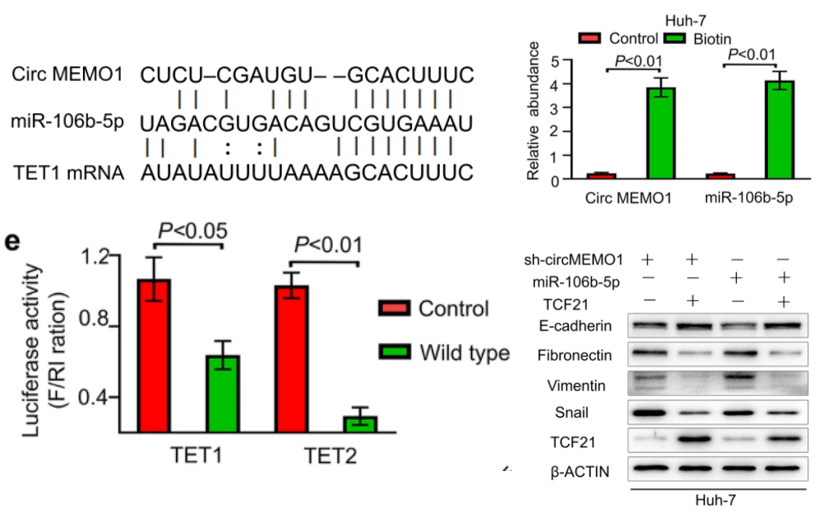
圖3:CircMEMO1 通過在 HCC 細胞中吸附 MiR-106b-5p 來調節 TET1/5hmC/TCF21 軸的水平
左上:circMEMO1與miR-106b-5p結合位點示意圖,miR-106b-5p與TET1 和 TET2結合位點示意圖。右上:circRNA RNA pull down qPCR顯示CircMEMO1與mir-106b-5p可以結合。
左下:双荧光素酶报告基因实验证实mir106b-5p與TET1/TET2的3’UTR直接結合。右下:rescue實驗表明TCF21過表達減弱由circMEMO1抑制或miR-106b-5p激活誘導的轉移特性和EMT過程。
circMEMO1 通過 miR-106b-5p/TET1/5hmC 軸調節 HCC 進展的機制示意圖
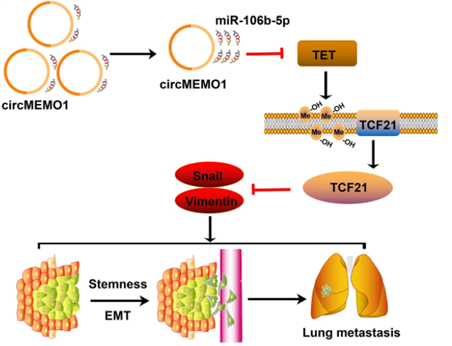
研究意義:
總之,在本研究中作者发现 CircMEMO1在肝癌轉移和幹細胞分化中是一個重要的腫瘤抑制因子,它通过miR-106b-5p/TET1/5hmC/TCF21軸和EMT過程發揮作用。作为一个关键的表观遗传修饰因子,CircMEMO1還可以調節肝癌細胞對索拉非尼治療的敏感性。
文章鏈接:
https://molecular-cancer.biomedcentral.com/articles/10.1186/s12943-021-01361-3

