
gdLTaqSTxhckcutbgUkwXhHkQKSvlEI
DreGnNFIeBzNxKz
UieptjfG
pdTmpoylxnLpx
bGVhoLrjbqnhixxTEiRVaLaWyrOiDnvzfIqlSzzpleIwxSgaoI
|
單細胞測序技術服務 靶向lncRNA单细胞全转录组测序 單細胞全轉錄組測序 |
|
生物分子凝聚體研究 HyPro靶RNA临近标记技术 |
|
RNA-蛋白相互作用 HyPro - MS CHIRP – MS RNA pull-down MS |
RNA-RNA/DNA相互作用 HyPro-seq/芯片 CHIRP-seq |
蛋白-RNA相互作用 AGO APP seq/芯片 RIP-RNA seq/芯片 |
蛋白-蛋白相互作用 RIME MS CoIP-MS |
|
NGS测序技术服务 R-loop 测序分析服务 |
|
NGS测序技术服务 環狀DNA测序 |
|
基因芯片技術服務 Small RNA修饰芯片 m6A单碱基分辨率芯片 mRNA&lncRNA表观转录组芯片 circRNA表观转录组芯片 |
NGS测序技术服务 表觀轉錄組學測序服務 RNA m6A甲基化测序(MeRIP Seq) |
LC-MS mRNA碱基修饰检测 tRNA碱基修饰检测 |
PCR技术服务 MeRIP-PCR技术服务 m6A绝对定量RT-PCR技术服务 m6A单碱基位点PCR(MazF酶切法)技术服务 |
|
Ribo-seq Ribo seq |
核糖體-新生肽链复合物(RNC) RNC联合 circRNA芯片 RNC联合 lncRNA芯片 RNC联合mRNA-seq |
|
蛋白表達定量 Label free非标定量技术 TMT标记定量技术 PRM靶向定量 |
山东大学副校长、齐鲁医学部部长陈子江院士团队长期从事生殖醫學、生殖内分泌及生殖遗传学的临床和相关基础研究。今年,该研究团队应用Arraystar lncRNA芯片在早發性卵巢功能不全病人的顆粒細胞中篩選到一個表達下調的lncRNA HCP5,该lncRNA分子通過抑制DNA損傷修復影響卵巢顆粒細胞凋亡。深入机制研究发现,lncRNA HCP5可以穩定蛋白YB1和ILF2的互作從而促進YB1入核。沉默lncRNA HCP5影響YB1的核定位及YB1與MSH5基因啓動子的結合,进而降低MSH5表達。因此,lncRNA HCP5通過與YB1互作調控MSH5轉錄及MSH5介導的DNA損傷修復,影响颗粒细胞功能,为早发性卵巢功能不全的疾病发生提供了新的表观遗传调控机制。該研究成果發表在Nucleic Acids Research(IF:11.147)上。(芯片實驗由给我免费播放片高清在线观看生物丨数谱生物提供技术服务)

研究背景
早發性卵巢功能不全(POI)的定义是40歲前出現閉經,主要表现为月经不调、促卵泡生成激素升高(FSH>25IU/I)及雌激素缺乏。早发性卵巢功能不全是常见的生殖内分泌紊乱,影响了约1-2%的育齡婦女。该病在临床上包括三个阶段:隐匿期、生化异常期和显性异常期。生化异常期病人(bPOI)有正常的月经,但FSH升高,生育能力下降。临床上POI病因複雜,涉及遗传、自身免疫、代谢和感染性因素,发病机制有待进一步阐明。在所有病例中,遗传缺陷导致疾病的约占20-25%,包括染色体缺陷和基因突变。POI相關基因的編碼區域變異導致的蛋白功能失常目前已被廣泛研究。 然而,蛋白编码基因区域仅占人类基因组的1.5%,研究者开始探索其他非编码RNA(例如miRNA、lncRNA、circRNA)的作用。
LncRNA是一類長度大於200nt,物种间保守性低的非编码RNA,通过改变染色质修饰、转录、mRNA降解、蛋白亚细胞定位调控蛋白编码基因表达,影响神经、内分泌、心血管系统的正常生理功能和疾病发生。
卵泡形成是一個複雜的過程,卵母细胞和体细胞的交流在卵泡发育过程中起着至关重要的作用。颗粒细胞(GCs)作为一种卵巢体细胞,为卵母细胞的发育和成熟提供必需的营养、生长因子和激素。颗粒细胞功能障碍会引起卵泡闭锁和细胞凋亡,并最终导致卵母细胞的丢失。目前,lncRNA在POI過程的作用未知,探索lncRNA在顆粒細胞中的作用有助於全面瞭解POI的發病機理。
本研究應用Arraystar lncRNA芯片在bPOI病人的顆粒細胞中篩選到一個表達下調的lncRNA HCP5,为POI相關基因MSH5的臨近基因。功能实验表明HCP5招募YB1調控MSH5表達,影响颗粒细胞DNA損傷修復。lncRNA HCP5作爲MSH5的轉錄調控因子,为POI提供了新的表觀調控機制。
技術路線

研究思路
LncRNA高通量篩選及PCR驗證
爲了探究POI過程中lncRNA的異常表達,作者利用Arraystar lncRNA芯片檢測了10個bPOI病人vs.10個同齡正常對照的卵巢顆粒細胞GCs中lncRNA表達變化,通过P<0.0005及FC>1.75篩選到159個差異表達lncRNA(Fig1A/B)。进一步通过与POI相關基因具有共定位或共表達關係縮小範圍,锁定POI相關基因MSH5上游276kb處的差異下調lncRNA HCP5並在20 bPOI vs. 22 control進行了擴大樣本驗證(Fig1C/D),HCP5已知與人類自身免疫疾病、感染、癌症相关,CPC2及CPAT分析確認HCP5爲非編碼RNA。FISH及分離核質RNA實驗證明HCP5定位於細胞核。
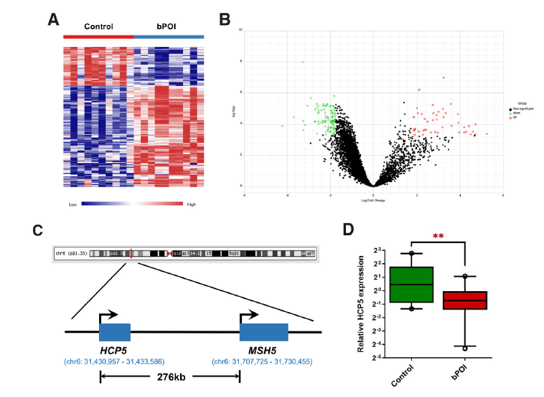
圖1. Arraystar Human lncRNA芯片篩選結果、HCP5染色體位置及qPCR驗證
A&B. 十對bPOI病人和同齡正常對照卵巢顆粒細胞GCs芯片篩選的差異表達lncRNA聚类图和火山图。
C.lncRNA HCP5在基因組上位於chr6 POI相關基因MSH5上游276kb處。
D.RT-qPCR擴大樣本(20 bPOI vs. 22 control) 驗證lncRNA HCP5在bPOI病人顆粒細胞中表達下調
功能研究有研究表明,lncRNA可以cis調控臨近基因表達,因此作者推测lncRNA HCP5可能cis調控MSH5表達。卵巢颗粒细胞系KGN中利用shRNA敲除HCP5,qPCR/WB檢測MSH5的mRNA及蛋白表達下調(Fig2A/B),且两者RNA具有共表達相關性。已知MSH5參與DNA雙鏈斷裂(DSBs)的同源重组修复,作者检测了卵巢颗粒细胞系KGN、COV434和SVOG,通过ETO促進DSBs後敲除HCP5,DNA雙鏈斷裂的標誌物 γH2AX增加,因此HCP5抑制DSBs(Fig2C);KGN細胞系中通過CPT促進DNA斷裂(只能被同源重组修复)后敲除HCP5,可以延长γH2AX出現至消失的時間從而延緩DSBs同源重組修復。敲除HCP5也可以促進卵巢顆粒細胞凋亡(Fig2D)。
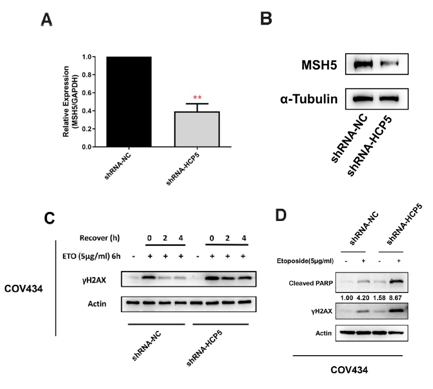
圖2. 敲除HCP5影響MSH5介導的DNA斷裂同源重組修復並促進卵巢顆粒細胞凋亡
A. 通過qPCR驗證敲除lncRNA HCP5抑制MSH5的mRNA表達。
B. 通過WB驗證敲除lncRNA HCP5抑制MSH5的蛋白表達。
C. 敲除lncRNA HCP5促進ETO誘導的DNA雙鏈斷裂。
D. 敲除lncRNA HCP5促進卵巢顆粒細胞凋亡。
爲了探究lncRNA HCP5結合的蛋白,作者利用RNA pull down富集HCP5結合的蛋白進行質譜檢測,发现HCP5可以結合YB1,利用YB1的抗體做RIP實驗反向驗證,可以富集到lncRNA HCP5(Fig3A/B)。qPCR/WB/免疫熒光實驗證明,敲除HCP5不會改變YB1表達量,但会抑制YB1入核(Fig3D)。已知ILF2可以結合YB1調控其核定位,RIP/Co-IP/IB實驗證明ILF2結合HCP5,敲除HCP5影響YB1與ILF2互作,推测HCP5可作爲YB1與ILF2的支架分子(Fig3C)。由于YB1可在細胞核內結合啓動子影響基因轉錄,作者进一步探究HCP5敲除是否影響YB1與臨近基因MSH5啓動子的結合。ChIP-qPCR證明YB1結合MSH5啓動子,敲除HCP5抑制YB1與MSH5啓動子結合(Fig4E)进而抑制MSH5的轉錄(Fig2A/B)。
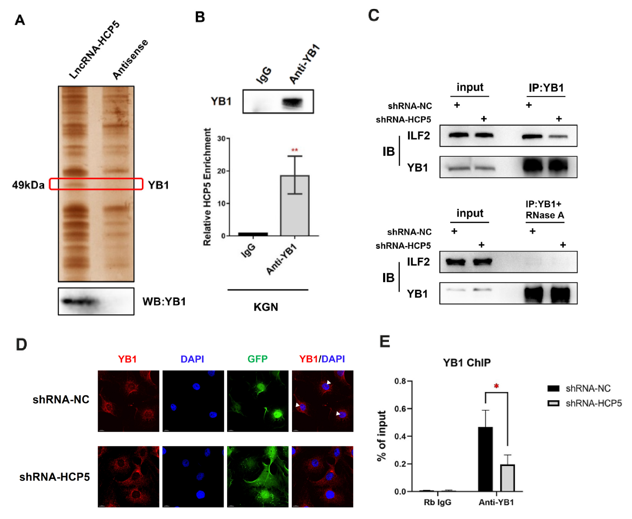
圖3. lncRNA HCP5作爲分子支架穩定YB1與ILF2互作,影响YB1覈定位及MSH5轉錄
A. RNA pull down實驗證明lncRNA HCP5結合蛋白YB1。
B. YB1 RIP實驗反向證明YB1結合lncRNA HCP5。
C. IB實驗證明敲除lncRNA HCP5影響YB1與ILF2的結合。
D. 免疫熒光實驗證明敲除lncRNA HCP5影響YB1的核定位。
E. ChIP實驗證明HCP5影響YB1與臨近基因MSH5 promoter的結合。
總結全文,研究结果表明,lncRNA HCP5在早發性卵巢功能不全病人的顆粒細胞中表達下調,lncRNA HCP5可以作爲支架分子,稳定蛋白YB1和ILF2的互作從而促進YB1覈定位,YB1入核後結合MSH5基因啓動子促進MSH5轉錄,进而影响DNA雙鏈斷裂同源重組修復和卵巢顆粒細胞凋亡,为早发性卵巢功能不全的疾病发生提供了新的表观遗传调控机制。
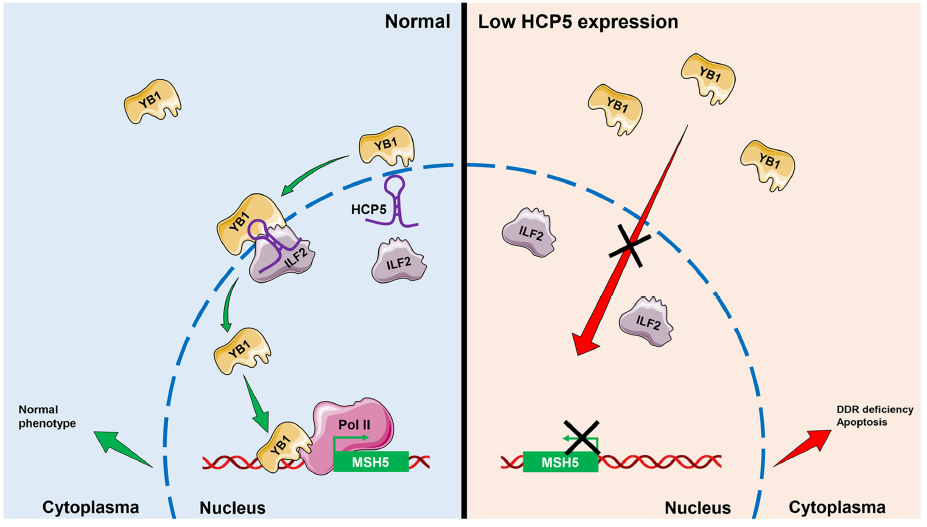
圖4. 早發性卵巢功能不全中HCP5降低,抑制YB1入核及MSH5轉錄,促进颗粒细胞凋亡
https://academic.oup.com/nar/article/48/8/4480/5766654
相關技術服務

