
VBFVSWvFDwNRBrXnfUCmcDYrKOpnRkjWUueVHk
ZSNriwFqSmSEhGQDigBAdRfkWnJ
uFKOlUFpFosTobuuHeoiEWiumfhewaYaITOmrQWOcTqNYlHDRarVGhpVFkRLmeYnZpiptEbucIvr
JJYAQnks
gsbDZgdcfVZAfiyrm
|
單細胞測序技術服務 靶向lncRNA单细胞全转录组测序 單細胞全轉錄組測序 |
|
生物分子凝聚體研究 HyPro靶RNA临近标记技术 |
|
RNA-蛋白相互作用 HyPro - MS CHIRP – MS RNA pull-down MS |
RNA-RNA/DNA相互作用 HyPro-seq/芯片 CHIRP-seq |
蛋白-RNA相互作用 AGO APP seq/芯片 RIP-RNA seq/芯片 |
蛋白-蛋白相互作用 RIME MS CoIP-MS |
|
NGS测序技术服务 R-loop 测序分析服务 |
|
NGS测序技术服务 環狀DNA测序 |
|
基因芯片技術服務 Small RNA修饰芯片 m6A单碱基分辨率芯片 mRNA&lncRNA表观转录组芯片 circRNA表观转录组芯片 |
NGS测序技术服务 表觀轉錄組學測序服務 RNA m6A甲基化测序(MeRIP Seq) |
LC-MS mRNA碱基修饰检测 tRNA碱基修饰检测 |
PCR技术服务 MeRIP-PCR技术服务 m6A绝对定量RT-PCR技术服务 m6A单碱基位点PCR(MazF酶切法)技术服务 |
|
Ribo-seq Ribo seq |
核糖體-新生肽链复合物(RNC) RNC联合 circRNA芯片 RNC联合 lncRNA芯片 RNC联合mRNA-seq |
|
蛋白表達定量 Label free非标定量技术 TMT标记定量技术 PRM靶向定量 |
近期,青島大學王昆教授發表名爲“The piRNA CHAPIR regulates cardiac hypertrophy by controlling METTL3-dependent N6-methyladenosine methylation of Parp10 mRNA”的研究性論文。该论文应用Arraystar Mouse piRNA芯片篩選鑑定出與心肌肥大相關的piRNA分子CHAPIR,並通過進一步機制研究檢測(如MeRIP seq等)發現該分子通過結合METTL3影响Parp10的甲基化來發揮調控功能。该研究成果于2020年10月發表在國際著名學術期刊Nature Cell Biology (IF: 17.728)上。(Arraystar piRNA芯片及MeRIP測序均由给我免费播放片高清在线观看生物丨数谱生物提供技术服务)
 |
研究背景
慢性心肌肥大及相關的心肌重塑是心臟功能障礙的主要影響因素,最终会导致严重的心衰和死亡。近期研究表明,mRNA的表觀遺傳修飾對心血管疾病的發展有重要影響,其中m6A是哺乳動物最主要的mRNA轉錄後修飾,可逆的m6A修飾對mRNA的剪切、稳定性、定位和翻译起着重要作用。已有研究证明m6A影響心臟生理和病理過程,然而,尚不清楚在肥厚性心肌细胞中m6A修飾失調的影響。
非編碼RNA(ncRNA)在生理和病理性心肌肥大中發揮獨特的調控功能,它们通过对基因的转录或转录后沉默来调控心肌肥大的分子互作网络。PiRNA是一類長26-32nt的小非編碼RNA,在生殖细胞中,piRNA結合PIWI蛋白介導轉座子和蛋白編碼基因的調控。尽管在心肌组织高丰度表达,但piRNA在心臟生理功能和疾病發生中作用仍然未知。在多能干细胞分化成心肌细胞过程中,piRNA具有動態和特異性表達模式;在心梗和心肌肥大等压力条件下,piRNA表達也發生了很大變化。
本次研究系統地探討了piRNA在病理性心肌肥大中的未知功能,揭示了piRNA通過結合m6A修飾酶METTL3影響RNA m6A修飾失調,从而介导肥大基因调控的潜在机制。
技術路線

研究思路
piRNA高通量篩選及驗證
爲了篩選到心肌肥大過程中差異表達的piRNA分子,作者应用Arraystar Mouse PiRNA芯片篩選了成年小鼠橫切主動脈縮窄(TAC)手术后4周獲得的左心室組織(心肌肥大模型组)与假手术对照组织中piRNA整體表達情況,并从中选择差异倍数前20的高丰度piRNA(原始信号>100)进行验证(图1A)。
在4 vs 4的樣本中qPCR驗證結果顯示,3個piRNA上調超過3倍,2個piRNA下調超過3倍。随后经过表达实验验证这3個上調piRNA對於心肌肥大標誌基因Myh7表達的影響以及q-PCR鑑定不同piRNA的組織特異性(图1B、C),作者锁定了一个在心脏中特异的且促进Myh7表達的piRNA分子DQ726659,並將其命名爲CHAPIR(心肌肥大相关piRNA)。
功能研究
爲了證明CHAPIR能夠促進心肌肥大的發生發展,首先作者在小鼠原代心肌细胞中敲低CHAPIR,發現原本由血管緊張素II刺激引發的Myh7上調的表型得到減弱,同時細胞表面積等相關指標也有所降低(图2A、B)。進一步的,在小鼠模型上的研究表明,敲除CHARIP能夠抑制由TAC手術引發的心肌肥厚現象(图2C),并且相关的标志基因等反映心肌肥厚程度的指标也有所降低。因此,CHAPIR對於心肌肥大的發生發展具有重要作用。
機制研究
進一步的,作者研究了CHAPIR促進心肌肥大的作用機制。首先,通过RNA pull down與質譜實驗聯用以及低通量驗證的方式,作者意外發現甲基化修飾轉移酶METTL3能夠與CHAPIR具有相互作用(图3A)。Dot blot實驗表明,敲除CHAPIR能夠顯著提高細胞內整體的m6A修飾水平(图3B)。为了找到CHAPIR影響下游基因甲基化的具體機制,作者利用MeRIP-seq(由给我免费播放片高清在线观看生物丨數譜生物提供技術服務),在CHAPIR過表達的小鼠心臟組織中找到六千多個具有差異m6A修飾的基因。接下來,利用m6A差異修飾數據與對應mRNA表達量差異數據進行聯合分析,作者找到了Parp10(图3C、D)。利用MeRIP-PCR实验發現,在過表達CHAPIR後,Parp10上的m6A修飾減少(图4A),同時Parp10的mRNA表達量上升(图4B),而敲低METTL3具有類似的現象(圖4C)。进一步的,作者通过western blot等實驗發現,Parp10能夠通過影響下游GSK3β的單ADP核糖基化(mono-ADP-ribosylation)以及NFATC4的細胞覈定位,從而影響心肌肥大的發生發展。
結果展示
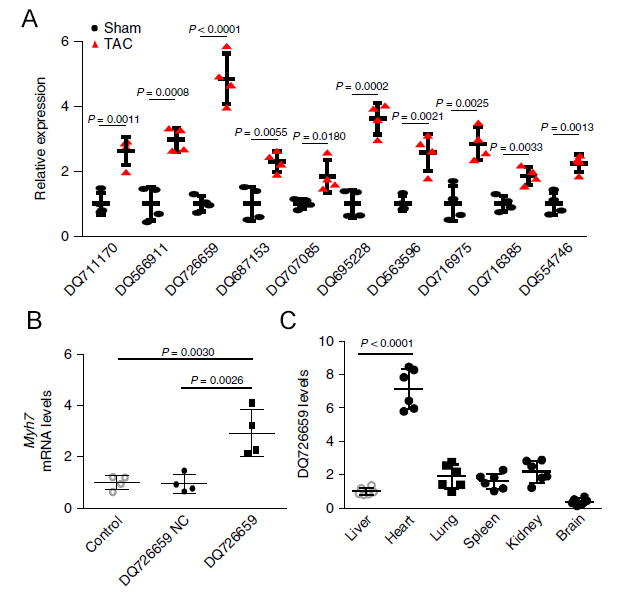
圖1. Arraystar Mouse PiRNA芯片篩選找到CHAPIR
A:Q-PCR验证Arraystar Mouse PiRNA芯片篩選得到的在TAC誘導心肌肥大小鼠模型中表達上調的前十個piRNA。B:Q-PCR检测心肌細胞中過表達CHAPIR(DQ726659)後心肌肥大標誌基因Myh7的表達情況。
C:Q-PCR驗證CHAPIR在不同組織中的表達情況。
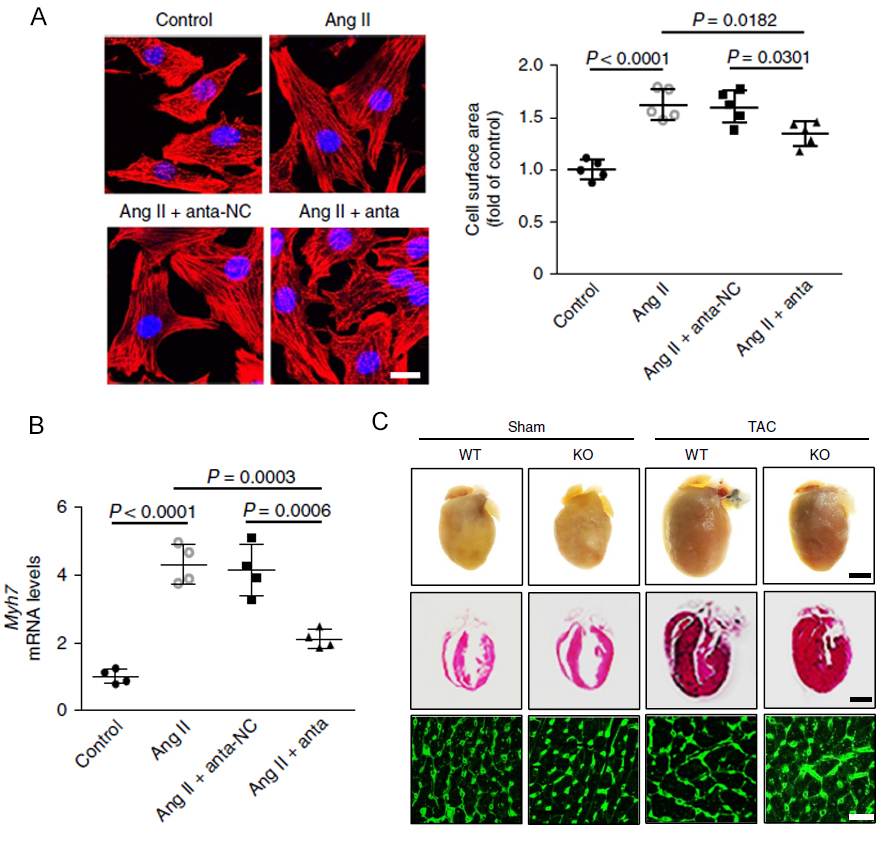
圖2. CHAPIR敲低抑制心肌肥大
A:免疫荧光檢測小鼠原代心肌細胞中敲低CHAPIR對細胞表面積的影響。B:Q-PCR检测小鼠原代心肌細胞中敲低CHAPIR對細胞內心肌肥大標誌基因myh7的表達情況的影響。C:在TAC處理誘導心肌肥大小鼠模型中,敲低CHAPIR回覆心肌肥大的表型。
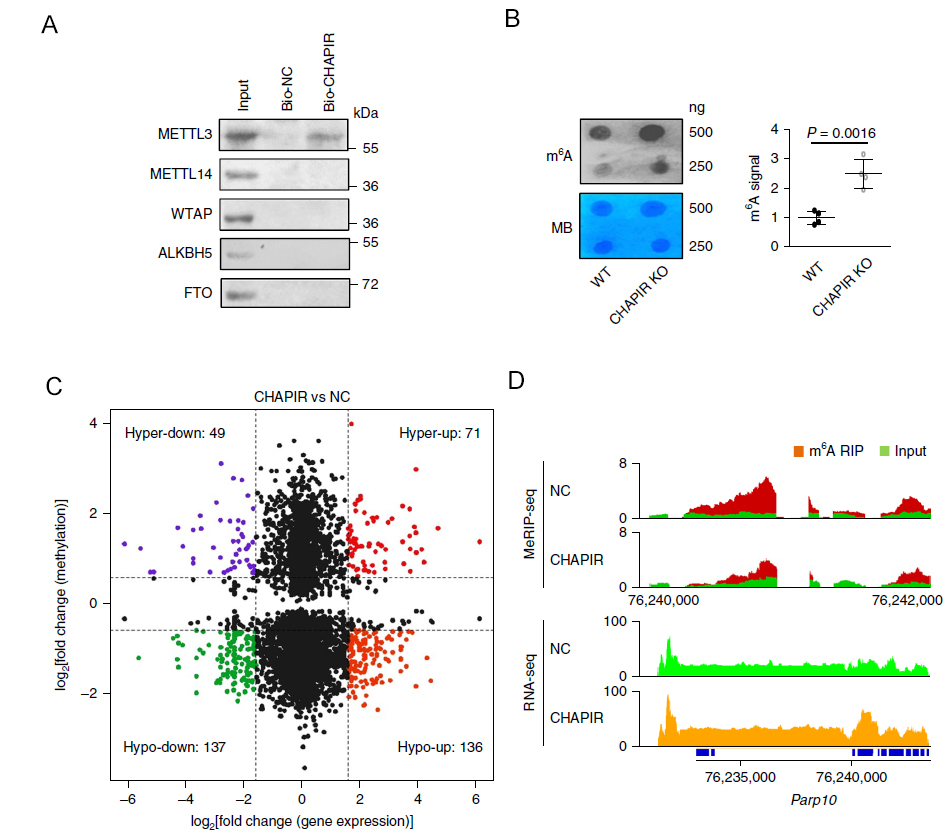
圖3. CHAPIR結合METTL3影響Parp10的m6A修飾
A:RNA pull down驗證CHAPIR能與METTL3結合。B:Dot blot實驗表明CHAPIR敲除能夠增強細胞內RNA的m6A修饰水平。C:取過表達CHAPIR的小鼠心臟組織與正常組織一起進行MeRIP-seq及RNA-seq實驗,將差異基因表達數據與差異m6A修饰變化數據進行聯合分析,最終找到Parp10。D:Parp10 mRNA上的m6A修饰变化情況與基因表達變化情況的可視化結果。
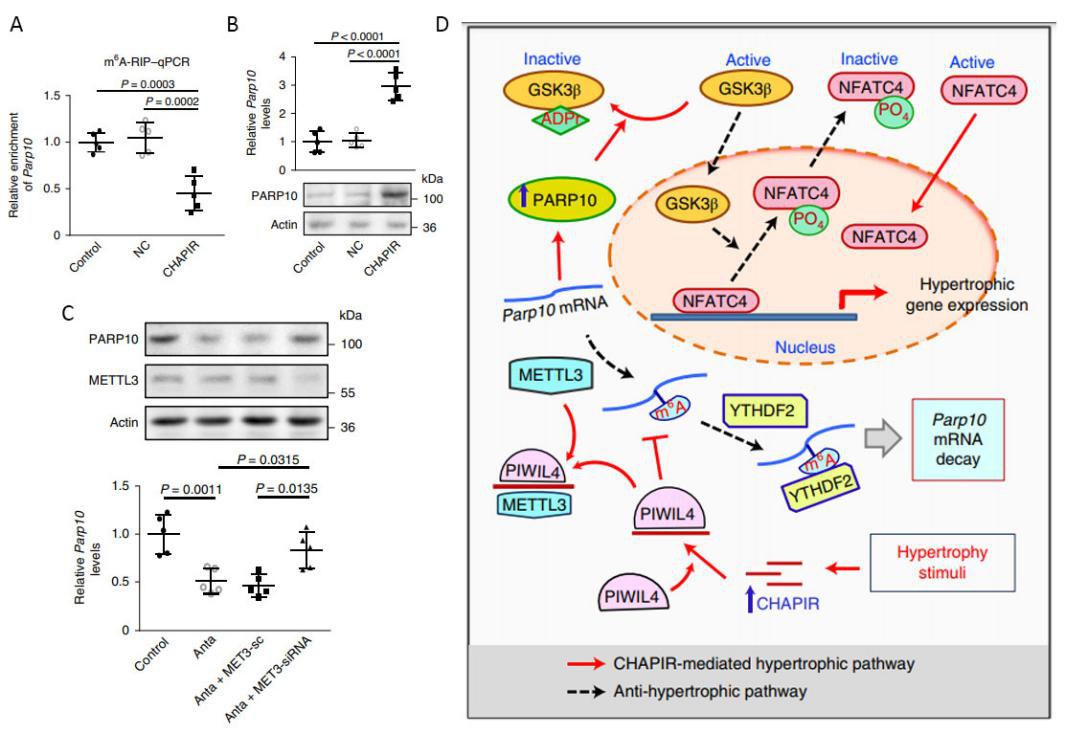
圖4. M6A修飾影響Parp10的穩定性
A:MeRIP-PCR验证過表達CHAPIR能夠降低Parp10的m6A修饰水平。B:Western blot檢測過表達CHAPIR後Parp10的mRNA變化情況。C:Q-PCR及western blot檢測敲低METTL3后Parp10的mRNA水平及蛋白水平變化情況。D:CHAPIR发挥促進心肌肥大的作用機制圖。在外界信號刺激下,piRNA分子CHAPIR的表達量升高,随后與PIWI蛋白及METTL3结合,導致Parp10的mRNA上m6A修飾減少,使Parp10的mRNA穩定性增加,进一步讓Parp10的蛋白表達量上升。表達量升高的Parp10能够通過影響GSK3β的單ADP核糖基化以及NFATC4的細胞內定位從而促進心肌肥大相關基因的表達。
研究意義:
作者利用Arraystar Mouse piRNA芯片在心肌肥大小鼠模型的心臟組織中找到了促進心肌肥大發生髮展的piRNA分子CHAPIR。细胞层面上的功能研究表明CHAPIR能够促進心肌細胞表達心肌肥大標誌基因myh7。小鼠模型上的功能研究則直接證明了CHAPIR能夠影響心肌肥大的表型。機制上,作者發現CHAPIR能夠通過結合甲基轉移酶METTL3,影響其下游基因Parp10的m6A修饰。而m6A修饰则能夠調節Parp10的mRNA穩定性,進一步影響該基因的蛋白表達,从而最终影响心肌肥大相關基因的表達情況以及相應的表型。總體而言,这项工作思路清晰,数据详实,为心肌肥大的治疗提供了新的思路与方法。
相關技術服務:

