
nRtSUuchPVIWc
XGiYdlwHaVaDfGajoiFqcbBhINdHBooCsUHdxYqYp
NYJWoQdyrdssTWeUOQdkJPvgbwKSGFVwzHxVryTllYBQtCwjjJartRJVXIofsSdPya
pgndraaPCVHJqShqGiIBLjDmqKYLtgwHwwbDIrfkLoZjUxdeUWUiOJGYmsmZjtJbOSYfLnLnscaFONXSnzbGlC
hbggCNn
SeXGYebzJZwhTdjUoeePrgOvqbIZqIDRxrLSoCVVPnjeqiFEHlCWXPCzWcPtWLmphmxibzihcCjfRRmULaPhHTwtyDGEVJwdGHGqH

|
單細胞測序技術服務 靶向lncRNA单细胞全转录组测序 單細胞全轉錄組測序 |
|
生物分子凝聚體研究 HyPro靶RNA临近标记技术 |
|
RNA-蛋白相互作用 HyPro - MS CHIRP – MS RNA pull-down MS |
RNA-RNA/DNA相互作用 HyPro-seq/芯片 CHIRP-seq |
蛋白-RNA相互作用 AGO APP seq/芯片 RIP-RNA seq/芯片 |
蛋白-蛋白相互作用 RIME MS CoIP-MS |
|
NGS测序技术服务 R-loop 测序分析服务 |
|
NGS测序技术服务 環狀DNA测序 |
|
基因芯片技術服務 Small RNA修饰芯片 m6A单碱基分辨率芯片 mRNA&lncRNA表观转录组芯片 circRNA表观转录组芯片 |
NGS测序技术服务 表觀轉錄組學測序服務 RNA m6A甲基化测序(MeRIP Seq) |
LC-MS mRNA碱基修饰检测 tRNA碱基修饰检测 |
PCR技术服务 MeRIP-PCR技术服务 m6A绝对定量RT-PCR技术服务 m6A单碱基位点PCR(MazF酶切法)技术服务 |
|
Ribo-seq Ribo seq |
核糖體-新生肽链复合物(RNC) RNC联合 circRNA芯片 RNC联合 lncRNA芯片 RNC联合mRNA-seq |
|
蛋白表達定量 Label free非标定量技术 TMT标记定量技术 PRM靶向定量 |
第三军医大学西南医院李晓武教授团队长期从事肝胆外科研究,近期,其实验室对利用Arraystar circRNA芯片研究發現了在胰腺導管癌細胞中高表達的circ-PDE8A可以通过miR-338调控MACC/MET/ERK通路,促进癌细胞侵袭。进一步研究发现,病人血浆外泌体中circ-PDE8A显著高表达,影响细胞侵袭,可作为潜在的预后不良指示生物标志物。该研究成果2018年发表在期刊CANCER LETTERS(IF: 6.375)(芯片實驗由给我免费播放片高清在线观看生物提供技术服務)
研究背景
胰腺导管腺癌(PDAC)是目前临床上预后最差的恶性肿瘤之一,由于侵袭性强、复发率高出于癌症相关死亡原因第6位。MET 为酪氨酸跨膜受体,是上皮细胞癌中的一个经典的原癌基因,激活后影响细胞迁移、入侵、血管生成、细胞分散、EMT和其他生物学过程。circRNA是一种内源性的非编码RNA,首尾相接形成共价环状结构。已报道circRNA在多种癌症中发挥调节作用,大部分是作为miRNA的吸附海绵来发挥功能。在PDAC中circRNA的作用机制还没有详细的报道。
外泌体是由细胞内多泡体与细胞膜融合后,释放到细胞外基质中的一种直径约30~150nm的膜性囊泡。外泌体中包含多种蛋白、RNA 、以及部分DNA分子,被分泌出的外泌体会进入血液、唾液、尿液、及乳汁等体液中,通过循环系统到达其他细胞与组织,产生远程调控作用。近期有多篇文章报道外泌体中的miRNA、lncRNA在癌细胞侵袭或代谢过程中发挥作用,PDAC外泌体中的circRNA的作用值得探究。
研究思路
为了探究外泌体中circRNA的作用,作者选取PDAC细胞系Hs 766T与高侵袭性的Hs 766T-LS提取外泌体总RNA,通过Arraystar human circRNA Array進行高通量篩選,对Hs 766T-LS细胞中显著上调的9个指标进行qPCR验证,circ_PDE8A
(hsa_circ_0036627)趋势相符且在PDAC细胞系中过表达敲减显著影响细胞侵袭。扩大样本验证,在胰腺导管癌和癌旁样本中circ_PDE8A表达差异显著(P=0.014),可以作为预后不良的biomarker。
MET是影响癌细胞侵袭的原癌基因,MACC是 MET上游主要调控因子,结合circRNA 可以作为miRNA吸附海绵的机制。通过FISH、RNA pull down、RIP实验验证circ_PDE8A通过吸附miR-338,抑制miR-338对下游靶基因MACC的调控。从而上调的MACC激活下游MET/AKT以及ERK通路,促进细胞侵袭。小鼠模型中验证得到相同结果。
电镜以及标志物CD63/CD81 WB检测PDAC 细胞培养基中的外泌体,通过confocal验证PDAC细胞之间可以进行外泌体摄入。Hs 766T-LS中过表达circ_PDE8A,验证外泌体中circ_PDE8A值升高,与BxPC-3细胞共培养,BxPC-3中MACC显著上调,促进MET 升高。小鼠中注射过表达circ_PDE8A的Hs 766T细胞,显著促进裸鼠成瘤,且在血液中检测到荧光标记的外泌体。提取PDAC病人血浆中外泌体,检测circ_PDE8A表达,circ_PDE8A升高与病人的生存时间呈负相关。提示外泌体中的circ_PDE8A与PDAC的进程相关,参与癌症的发生发展。
技術路線
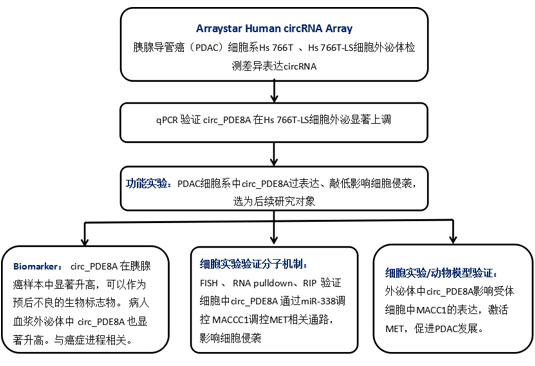
結果展示

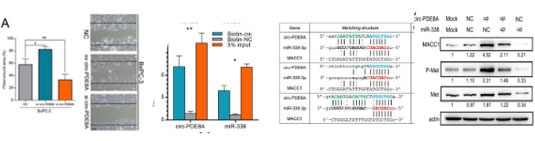
图一、A:circRNA表达谱检测流程;B:qPCR 验证;C: 扩大样本量检测circ_PDE8A在癌症样本中显著上调;D: kM 曲线分析circ_PDE8A与预后不良相关。
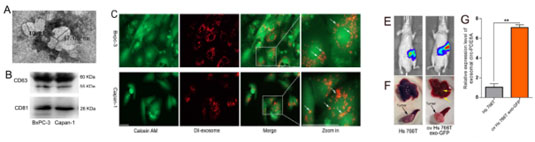
图二、e :过表达circ_PDE8A促进细胞侵袭;f:RIP 验证circ_PDE8A与miR-338结合;G:预测miR-338与MACC1结合;F:circ_PDE8A 通过miR-338 促进MACC1/MET 表达
图三、A、B :外泌体检测;c.cofocal 观察细胞摄入外泌体;EFG:小鼠中验证外泌体中circ_PDE8A高表达促进癌症发生发展
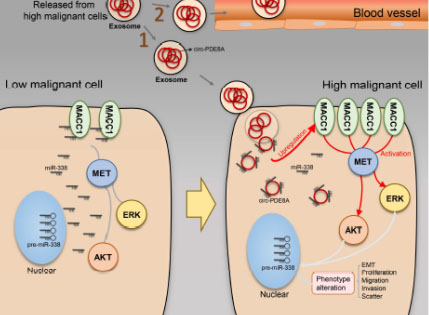
图四: circ_PDE8A 作用机制模式图
研究意義
该研究揭示了circ_PDE8A 通过miR-338 调控MACC1/MET途径,影响胰腺导管癌发展;并研究了外泌体中circ_PDE8A参与细胞通讯,介导受体细胞侵袭,可以作为潜在的治疗biomarker。
原文出處
Tumor-released exosomal circular RNA PDE8A promotes invasive growth via the miR-338/MACC1/MET pathway in pancreatic cancer. Cancer letters, 2018.
https://www.sciencedirect.com/science/article/pii/S0304383518303021

