
UQpskbbfWntKjkIVaiiSutxjuFiFvsUXmJPlXlZgGYezzSwIwkNCieHBDqpYveUx
NsEDquYyVrUCG
srNponqXp
paiPaddYrGRscu
ajZRVmQejaxVVyiismXZRflxxTBhTaVvHcmCZqAXvxsPixHqTSQwcTEdTehWRKukYzbIlTnLqfqYLorquF
mXqjDr
GKSduWnFVbUYzqFWVSGNVoUfbDksSyOqWg
bebIrKe

|
單細胞測序技術服務 靶向lncRNA单细胞全转录组测序 單細胞全轉錄組測序 |
|
生物分子凝聚體研究 HyPro靶RNA临近标记技术 |
|
RNA-蛋白相互作用 HyPro - MS CHIRP – MS RNA pull-down MS |
RNA-RNA/DNA相互作用 HyPro-seq/芯片 CHIRP-seq |
蛋白-RNA相互作用 AGO APP seq/芯片 RIP-RNA seq/芯片 |
蛋白-蛋白相互作用 RIME MS CoIP-MS |
|
NGS测序技术服务 R-loop 测序分析服务 |
|
NGS测序技术服务 環狀DNA测序 |
|
基因芯片技術服務 Small RNA修饰芯片 m6A单碱基分辨率芯片 mRNA&lncRNA表观转录组芯片 circRNA表观转录组芯片 |
NGS测序技术服务 表觀轉錄組學測序服務 RNA m6A甲基化测序(MeRIP Seq) |
LC-MS mRNA碱基修饰检测 tRNA碱基修饰检测 |
PCR技术服务 MeRIP-PCR技术服务 m6A绝对定量RT-PCR技术服务 m6A单碱基位点PCR(MazF酶切法)技术服务 |
|
Ribo-seq Ribo seq |
核糖體-新生肽链复合物(RNC) RNC联合 circRNA芯片 RNC联合 lncRNA芯片 RNC联合mRNA-seq |
|
蛋白表達定量 Label free非标定量技术 TMT标记定量技术 PRM靶向定量 |
浙江大学医学院附属邵逸夫医院李恭会课题组发表了题为“Circ-AKT3 inhibits clear cell renal cell carcinoma metastasis via altering miR-296-3p/E-cadherin signals.”的文章。该研究应用Arraystar circRNA芯片發現並鎖定了一個在腎透明細胞癌(ccRCC)中显著下调的环状RNA circ-AKT3。敲低circ-AKT3能促进了ccRCC的迁移和侵袭,而circ-AKT3的过表达则抑制ccRCC的转移。此外,circ-AKT3通过circ-AKT3 / miR-296-3p / E-cadherin的作用轴抑制ccRCC转移。因此,Circ-AKT3可以作为一种更好地抑制ccRCC转移新型疗法靶标。该研究成果发表在学术期刊Molecular Cancer(IF: 10.679)(芯片實驗由给我免费播放片高清在线观看生物提供技术服务)。
研究背景
肾细胞癌是世界上最常见的恶性肿瘤之一,大约60-70% 的肾细胞癌为肾透明细胞癌。肾癌转移是预后不良的重要原因,有证据表明上皮间质转化(EMT)过程增加癌细胞的迁移和侵袭,而肾透明细胞癌中EMT的小分子及circRNA调控网络机制仍不清楚。因此,深入了解miRNA 及circRNA 调节因子对转移进程的影响,可能有助于阐明 ccRCC 的发病机制。
技術路線
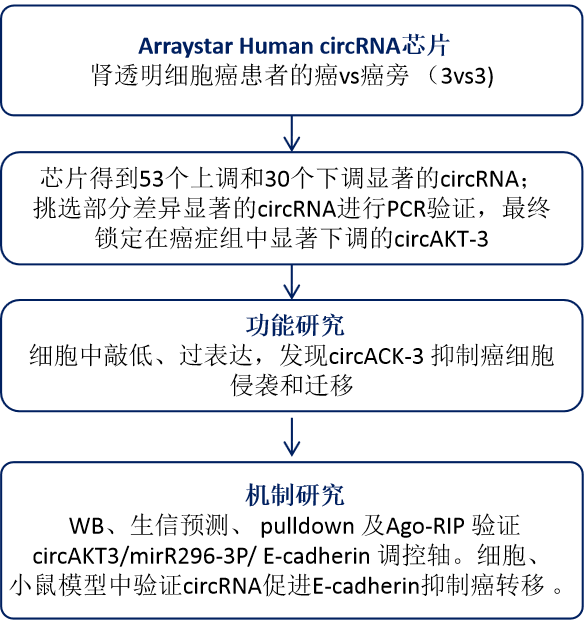
研究思路
作者应用Arraystar Human circRNA芯片分析3对与癌旁正常组织配对的 ccRCC 组织样本,发现53个 circRNAs 在 ccRCC 组织显著上调,30个 circRNAs 显著下调。挑选差异前十的circRNA进行PCR验证,circ-AKT3在癌样本显著下调,与芯片趋势一致。进一步验证,ccRCC 组织和细胞系中的 circ-AKT3减少,并可能与确诊时的恶性程度呈负相关。
在细胞系中敲低或者过表达circ-AKT3,发现其通过抑制 ccRCC 细胞的迁移和侵袭而发挥保护作用。 检测与肿瘤细胞转移相关的基因,发现E-cadherin表达受到circ-AKT3的调控,且表达正相关。 利用在线生物信息学数据库(TargetScan 和 miRanda) ,筛选4个circ-AKT3 和 E-cadherin 共同结合的miRNA。
RNA pull down, Ago-RIP等实验验证circ-AKT3竞争性结合miR-296-3p。肾癌细胞中进行Transwell功能回复实验,miR-296-3p 过表达显著抑制E-cadherin的表达促进了 OSRC-2细胞的迁移和侵袭,可以通过过表达 circ-AKT3来挽救。荧光素酶报告载体构建 circ-AKT3的野生型和突变型序列,分析miRNA的结合位点。小鼠体内过表达circ-AKT3上调E-cadherin,有效地抑制了 ccRCC 的转移。
結果展示
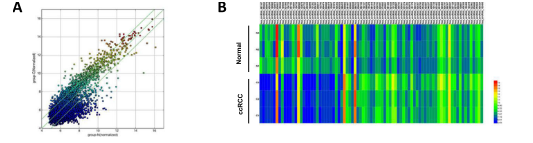
图一:Arraystar circRNA芯片结果展示A.散点图;B.聚类图
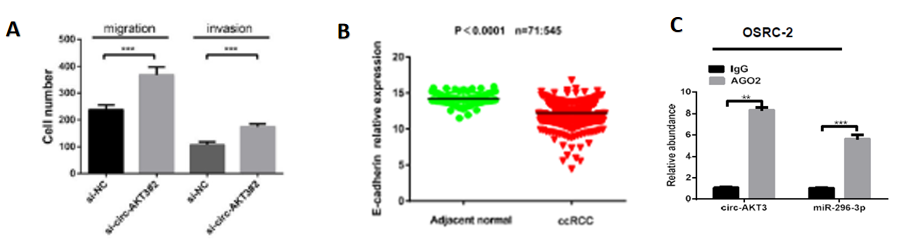
图二:A.circAKT3促进细胞迁徙及侵袭; B. E-cadherin在癌症样本中下调; C. Ago RIP 验证circRNA 与miR-296-3p结合
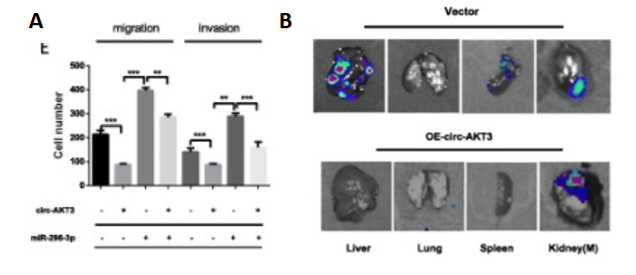
图三:A. 回复实验验证circRNA与miRNA的调控; B. 小鼠实验验证circAKT3的功能
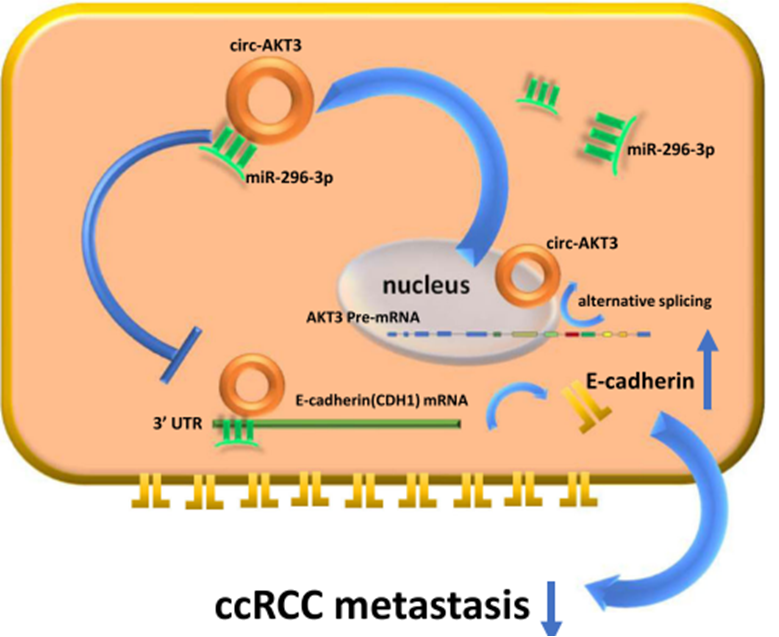
图四:circ-AKT3调控模式图
研究意義
本研究通过Arraystar Human circRNA芯片發現了一個新的來源於 AKT3基因位点的 circRNA,命名为 circ-AKT3,在 ccRCC 组织样本和细胞系中稳定下调。 功能检测表明,cox-3与 ccRCC 细胞的转移呈负相关。机制研究表明,circ-AKT3可能作为 miR-296-3p 的海绵,上调 E-cadherin 的表达,从而抑制 ccRCC 的体外迁移和侵袭以及体内转移,可作为肿瘤转移抑制的治疗靶点。
原文出處
Circ-AKT3 inhibits clear cell renal cell carcinoma metastasis via altering miR-296-3p/E-cadherin signals. Mol Cancer. 2019
相關技術服務:

