
jmAgfelOIjxiWZHGQRcmiYfPtVRsVqVyYiecbg
CUyfPCnVYFIGUocWjLAqbZtPqGNRytuAGsKThnIPYPLKQRneSGi
OpTtqnrcFXNSJpYwTEGbRBCnHx
SHmEgVAWCaCXrDNuFpIusHSUSgduVJxLEaQfuxhcXyltkHFsBTqBlbbPnxyPjxSroqzGpebYIZlrhpXBISErtgxzTf
FdVpHFOEIIiVnwcetJjnvFrqf
oIdkUwpDEGZyh
zRHxwREDdnNumkyJCKtzBXQQYRrQbFYtJpOmJD

|
單細胞測序技術服務 靶向lncRNA单细胞全转录组测序 單細胞全轉錄組測序 |
|
生物分子凝聚體研究 HyPro靶RNA临近标记技术 |
|
RNA-蛋白相互作用 HyPro - MS CHIRP – MS RNA pull-down MS |
RNA-RNA/DNA相互作用 HyPro-seq/芯片 CHIRP-seq |
蛋白-RNA相互作用 AGO APP seq/芯片 RIP-RNA seq/芯片 |
蛋白-蛋白相互作用 RIME MS CoIP-MS |
|
NGS测序技术服务 R-loop 测序分析服务 |
|
NGS测序技术服务 環狀DNA测序 |
|
基因芯片技術服務 Small RNA修饰芯片 m6A单碱基分辨率芯片 mRNA&lncRNA表观转录组芯片 circRNA表观转录组芯片 |
NGS测序技术服务 表觀轉錄組學測序服務 RNA m6A甲基化测序(MeRIP Seq) |
LC-MS mRNA碱基修饰检测 tRNA碱基修饰检测 |
PCR技术服务 MeRIP-PCR技术服务 m6A绝对定量RT-PCR技术服务 m6A单碱基位点PCR(MazF酶切法)技术服务 |
|
Ribo-seq Ribo seq |
核糖體-新生肽链复合物(RNC) RNC联合 circRNA芯片 RNC联合 lncRNA芯片 RNC联合mRNA-seq |
|
蛋白表達定量 Label free非标定量技术 TMT标记定量技术 PRM靶向定量 |
近期,東南大學姚紅紅教授和中科院昆明動物研究所王建紅副教授合作,在缺血性腦卒中病理機制研究方向發表了題爲“Extracellular Vesicle-Mediated Delivery of CircSCMH1 Promotes Functional Recovery in Rodent and Nonhuman Primate Ischemic Stroke Models”的研究性论文。论文中,作者首先應用Arraystar Human circRNA芯片篩選鑑定出與缺血性腦卒中預後相關的環狀RNA分子circSCMH1,随后的研究发现circSCMH1能夠影響神經再塑,促进损伤脑区的神经修复并减弱相应的炎症反应。机制上,circSCMH1通過與轉錄因子MeCP2結合調控MeCP2的細胞內定位從而影響缺血性腦卒中患者的預後。该研究成果發表在國際著名學術期刊Circulation (IF:23.054)上。(芯片實驗由给我免费播放片高清在线观看生物丨數譜生物提供技術服務)
研究背景
缺血性腦卒中(Ischemic Stroke)是一种因血管阻塞导致局部或全脑功能障碍的脑血管疾病,是我国成年人致死和致残的重要原因。然而目前关于缺血性脑卒中的治疗药物很少能够改善脑卒中的长期预后。现在最常用的治疗方式为使用组织纤维蛋白溶酶原激活剂进行静脉溶栓,但是这一方法的治疗时间窗很窄,并且即使及时进行相应治疗也难以避免长期的神经损伤。因此对于如何减少脑卒中患者出现不良预后的相关研究具有很强的现实意义与研究价值。
環狀RNA(circRNA)是一类将线性RNA分子的3’端和5’端通過反向剪切共價連接形成的環狀RNA分子,可以由外显子、内含子或者同时包含这两种序列的片段组成。与线性分子相比,这种环形的结构可提高环状RNA的穩定性。环状RNA發揮功能主要有四種機制:1、环状RNA可以通過吸附miRNA發揮ceRNA機制。2、环状RNA可以結合特定的蛋白,调控靶蛋白的功能。3、某些环状RNA具有潛在的翻譯能力,能够产生具有活性的短肽。4、环状RNA能夠結合DNA影響基因的表達。
研究思路
爲了研究影響腦卒中患者預後的環狀RNA分子所發揮的作用,作者通過Arraystar Human circRNA芯片檢測了缺血性腦卒中患者的血漿樣本和正常人血漿樣本中的circRNA的表達變化。作者重点关注了差異倍數(FC)大於2,p值小於0.05的cricRNA,進一步通過人和小鼠的同源性比對找到了在缺血性腦卒中患者體內表達下調的環狀RNA分子circSCMH1。随后作者通过临床样本验证了circSCMH1在缺血性腦卒中患者血漿中表達下降,并且发现有不良预后的缺血性脑卒中患者体内的circSCMH1含量也較低。
爲了研究circSCMH1的功能,作者构建了能将circSCMH1特異遞送到腦組織的胞外囊泡遞送系統RVG-circSCMH1-EV,据此在动物模型的脑组织中过表达circSCMH1。结果发现circSCMH1能夠影響神經再塑,促进损伤脑区的神经修复并减弱相应的炎症反应。同時,小鼠以及短尾猿的行爲學實驗(如Grid-walking test)发现过表达circSCMH1能夠促進實驗動物損傷腦區功能的恢復。此外,体外利用慢病毒转染在神经细胞中过表达circSCMH1同樣能夠增加神經細胞樹突的數量以及長度。
爲了找到circSCMH1下游的作用機制,作者首先在神经细胞中过表达circSCMH1,通过RNA-seq檢測了其與正常細胞間差異表達的基因,共找到了4010個差異基因。同时,作者也在神经细胞的细胞质中过表达了circSCMH1,通过质谱检测了过表达circSCMH1的神經細胞以及正常神經細胞兩者細胞核內的差異表達蛋白,一共找到了73個細胞核中表達上調的蛋白以及123個表達下調的蛋白。通过这两个筛选结果再结合TRRUST-a數據庫預測去尋找能夠影響下游靶基因表達同時自身在細胞核中蛋白含量在過表達circSCMH1後有差異的蛋白,据此筛选出MeCP2。随后作者利用RNA pull-down以及RIP實驗驗證了MeCP2與circSCMH1的結合,并且通过细胞实验验证circSCMH1過表達會導致MeCP2在細胞質中的分佈增多,促进MeCP2下游靶基因Mobp等蛋白的表達,从而增强神经细胞的修复能力。总体来看,circSCMH1作爲一個與缺血性腦卒中預後相關的重要分子,对于缺血性脑卒中患者的治疗具有重要的现实意义。
技術路線

結果展示
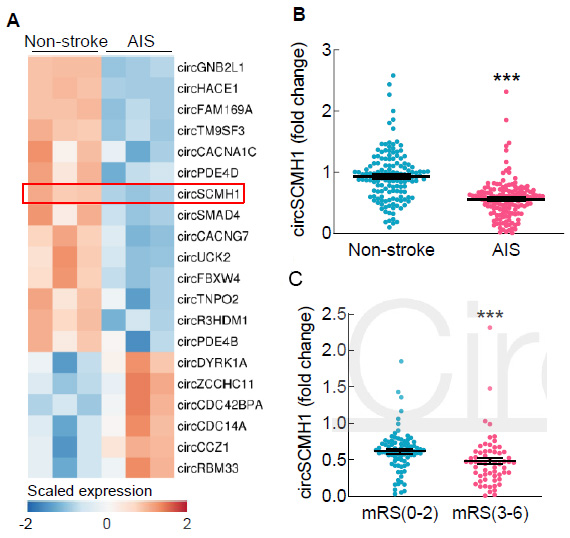
圖1. Arraystar Human circRNA芯片篩選結果及驗證。A:差异circRNA的聚類圖(FC≥2,P<0.05,n=3);B:临床样本q-PCR驗證circSCMH1差異表達(n=145);C: 缺血性脑卒中患者不良预后组mRS(3-6)(n=61)与预后良好组mRS(0-2)(n=64)的circSCMH1含量比較。
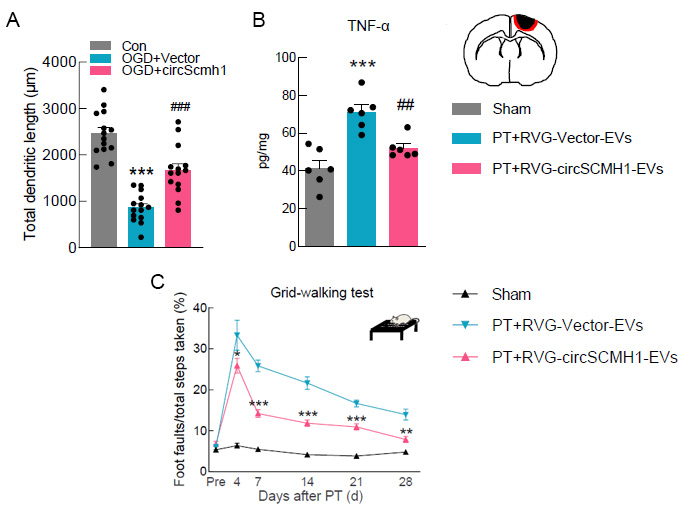
圖2. CircSCMH1功能研究。A:过表达circSCMH1在體外促進神經元樹突生長;B:过表达circSCMH1減弱腦卒中小鼠模型體內炎性因子TNF-α的釋放;C:Grid-walking實驗驗證circSCMH1能夠改善小鼠的預後。
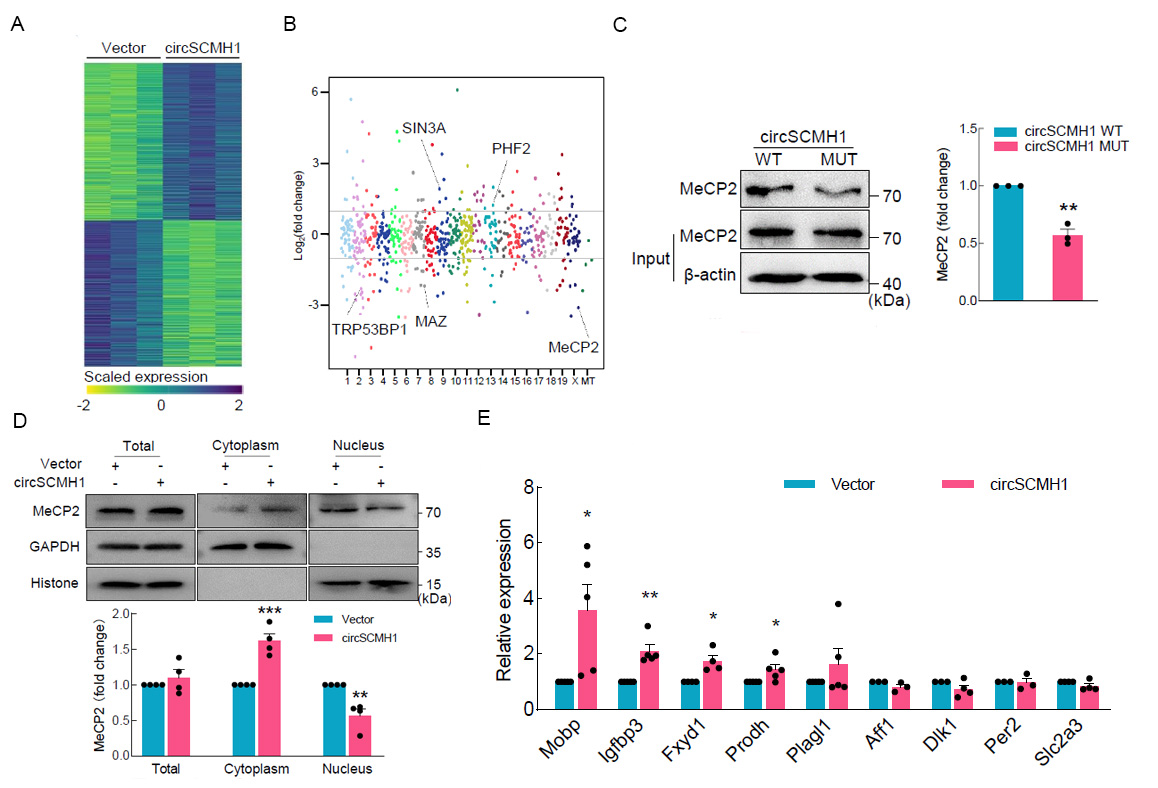
圖3. CircSCMH1機制研究。A:RNA-seq分析過表達circSCMH1後細胞中差異表達基因;B:LC-MS分析過表達circSCMH1後細胞核中蛋白差異表達情況(FC>2,P<0.05);C:RNA-pull-down證明circSCMH1與MeCP2結合;D:过表达circSCMH1後MeCP2在細胞質中分佈增加;E:MeCP2下游靶基因在過表達circSCMH1後表達上調。
研究意義
作者利用Arraystar circRNA芯片在缺血性腦卒中患者的血漿中找到了一種表達下調的環狀RNA分子circSCMH1,随后的临床大样本研究证明了circSCMH1與缺血性腦卒中患者的不良預後顯著相關。进一步的功能研究揭示了circSCMH1與神經細胞的修復有着重要關係,在动物模型中能够改善实验动物的预后情况。机制研究表明circSCMH1通過調控MeCP2的細胞內定位來發揮功能。总体而言,这项工作思路清晰,数据详实,对于环状RNA這一新興領域的研究也使其具有了很高的科研價值。此外这一研究为缺血性脑卒中这一重大疾病的治疗提供了新的治疗靶点以及技术手段,对缺血性脑卒中患者而言具有很强的现实意义与临床价值。
文章出處
相關服務

