
yFIisdrusFjnNV
qDmRlqWIRYHZBoVnGhbRlDLtzY
TxtGpBRJpkVWLCx
ifsGCeSuHifWhqtkNzJGInhY
XJhghcdkGvuwQX

|
單細胞測序技術服務 靶向lncRNA单细胞全转录组测序 單細胞全轉錄組測序 |
|
生物分子凝聚體研究 HyPro靶RNA临近标记技术 |
|
RNA-蛋白相互作用 HyPro - MS CHIRP – MS RNA pull-down MS |
RNA-RNA/DNA相互作用 HyPro-seq/芯片 CHIRP-seq |
蛋白-RNA相互作用 AGO APP seq/芯片 RIP-RNA seq/芯片 |
蛋白-蛋白相互作用 RIME MS CoIP-MS |
|
NGS测序技术服务 R-loop 测序分析服务 |
|
NGS测序技术服务 環狀DNA测序 |
|
基因芯片技術服務 Small RNA修饰芯片 m6A单碱基分辨率芯片 mRNA&lncRNA表观转录组芯片 circRNA表观转录组芯片 |
NGS测序技术服务 表觀轉錄組學測序服務 RNA m6A甲基化测序(MeRIP Seq) |
LC-MS mRNA碱基修饰检测 tRNA碱基修饰检测 |
PCR技术服务 MeRIP-PCR技术服务 m6A绝对定量RT-PCR技术服务 m6A单碱基位点PCR(MazF酶切法)技术服务 |
|
Ribo-seq Ribo seq |
核糖體-新生肽链复合物(RNC) RNC联合 circRNA芯片 RNC联合 lncRNA芯片 RNC联合mRNA-seq |
|
蛋白表達定量 Label free非标定量技术 TMT标记定量技术 PRM靶向定量 |
中山大學孫逸仙紀念醫院蘇士成教授、許小丁教授與中山大學附屬第三醫院高志良教授合作,在非酒精性脂肪性肝炎領域發表了題爲“Targeting Mitochondria-Located circRNA SCAR Alleviates NASH via Reducing mROS Output”的研究性論文。该论文应用Arraystar Human CircRNA芯片篩選鑑定出與非酒精性脂肪性肝炎發生相關的環狀RNA分子SCAR,功能研究表明,在线粒体中过表达circRNA SCAR會抑制肝臟成纖維細胞的活化並抑制相應的炎症反應,敲低则有相反的表型。机制研究发现,由脂质暴露引发的内质网应激(ER stress)会上调CHOP的表達,CHOP通過抑制PGC-1α的转录从而导致线粒体中circRNA SCAR表達量的下降。circRNA SCAR表達量的下降使得原本與其結合的ATP5B轉而與CypD結合導致mPTP通道開放。开放的mPTP通道能夠使線粒體中的ROS釋放到細胞質中,而ROS作爲一類活性氧物質能夠增強肝臟成纖維細胞的促炎能力從而導致肝臟炎症的加重。总体而言,该研究解决了非酒精性脂肪性肝炎发生发展机制的重要问题,发现了线粒体circRNA的重要功能並發展了一系列相關的實驗方法,为后续研究奠定了基础并指明了方向。該研究成果於2020年10月發表在國際著名學術期刊Cell (IF: 38.637)上。(芯片實驗由给我免费播放片高清在线观看生物丨数谱生物提供技术服务)
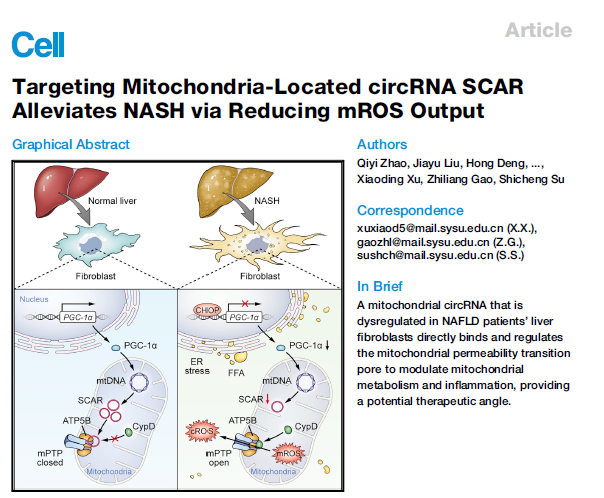
研究背景
非酒精性脂肪性肝炎(NASH)属于脂肪肝病的一种,相比于单纯性肝脂肪变性,该病引发的肝损伤更加严重,患者易于出现肝纤维化并引发相关肝脏疾病如肝硬化甚至肝癌的产生。据报道称,非酒精性脂肪性肝炎的全球患病率大约在3%-5%。因此,對該病的研究具有重要的科學意義和應用價值。
環狀RNA(circRNA)是一类将线性RNA分子的3’端和5’端通過反向剪切共價連接形成的環狀RNA分子,可以由外显子、内含子或者同时包含这两种序列的片段组成。与线性分子相比,这种环形的结构可提高环状RNA的穩定性。环状RNA發揮功能主要有四種機制:1、环状RNA可以通過吸附miRNA發揮ceRNA機制。2、环状RNA可以結合特定的蛋白,调控靶蛋白的功能。3、某些环状RNA具有潛在的翻譯能力,能够产生具有活性的短肽。4、环状RNA能夠結合DNA影響基因的表達。
技術路線

研究思路
1. CircRNA高通量篩選及臨牀數據研究
爲了研究影響非酒精性脂肪性肝炎(NASH)發生的具體機制,作者选取了四份NASH患者肝成纖維細胞樣本,通过与正常样本进行对比,采用Arraystar Human CircRNA芯片篩選了差異倍數大於2,P值小於0.05的指標(图1A)。由于ROS的主要來源是線粒體,故作者重點尋找了線粒體定位的環狀RNA,最終找到在NASH患者肝成纖維細胞線粒體中表達下調的環狀RNA分子SCAR(图1B),並通過RNase R消化、免疫荧光等实验验证了这一点(图1C)。进一步,通过对临床数据的分析,结果表明肝成纤维细胞中环状RNA分子SCAR的水平與其細胞內ROS含量呈反比且和整體肝臟健康程度呈正相關關係(图1D),表明SCAR確實可能與NASH的發生相關。
2. 功能研究
爲了證實環狀RNA分子SCAR具有引發NASH的功能,作者在肝成纖維細胞線粒體中過表達了這一環狀RNA。通过ELISA等實驗表明,过表达SCAR後,肝成纖維細胞內從線粒體釋放到細胞質中的ROS量明顯減少(图2A),并且能够抑制肝成纖維細胞的活化以及炎症因子的釋放(图2B、2C、2D)。此外,敲低該分子則有相反的表型。除了细胞实验外,作者在小鼠模型上通过免疫组化等实验发现过表达SCAR使肝部浸潤巨噬細胞減少(图2E)。因此,SCAR確實具有抑制NASH的能力並具有潛在的治療價值。
3. 機制研究
進一步的,针对SCAR引發NASH的下游機制這一問題。首先作者通过RNA pull down與質譜聯用的方式找到了SCAR的結合蛋白ATP5B並確定了它們間的結合區域(图3A、3B)。已有文献表明,ATP5B作爲線粒體上mPTP通道的組成蛋白之一,可以影响该通道的开放程度,因此作者利用IP等技術深入研究了SCAR對於mPTP通道的影響。结果发现:环状RNA分子SCAR能夠阻礙CypD蛋白結合ATP5B,从而导致mPTP通道無法開放(图3C)。因此,在SCAR表達量減少的情況下,mPTP通道能夠被CypD結合並開啓,从而使得线粒体内的ROS釋放到細胞質中(图3D),進而導致肝成纖維細胞的細胞因子釋放減少(图3E)。
最後,作者進一步研究了調控SCAR表達量的上游機制。通过CLIP-seq、RIP及q-PCR實驗表明,肝成纤维细胞在脂质暴露的情况下发生的内质网应激(ER stress)导致CHOP蛋白表達量下降,進一步使PGC-1α表達量下降(图4A),PGC-1α通過調控轉錄(图4B),从而最终使得SCAR的表達降低(图4C)。
結果展示
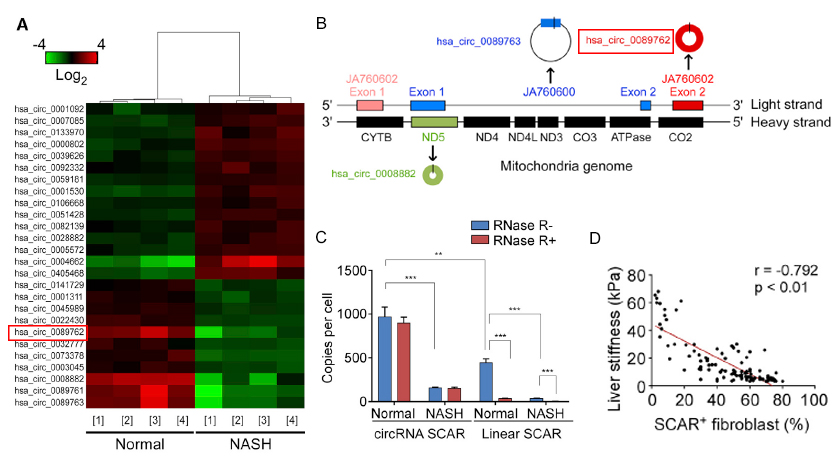
圖1. Arraystar Human CircRNA芯片篩選及驗證結果。
A:差異circRNA聚類圖(FC≥2,P<0.05,n=4),在NASH模型病人中找到一個明顯下調的環狀RNA分子SCAR(hsa_circ_0089762)。B:SCAR对应在线粒体基因組上的位置(以红框標註)。C:Rnase R处理后,Q-PCR驗證SCAR的環狀結構以及SCAR在NASH患者中的表達情況。D:NASH患者肝臟硬度與SCAR成纖維細胞數目的相關性分析。
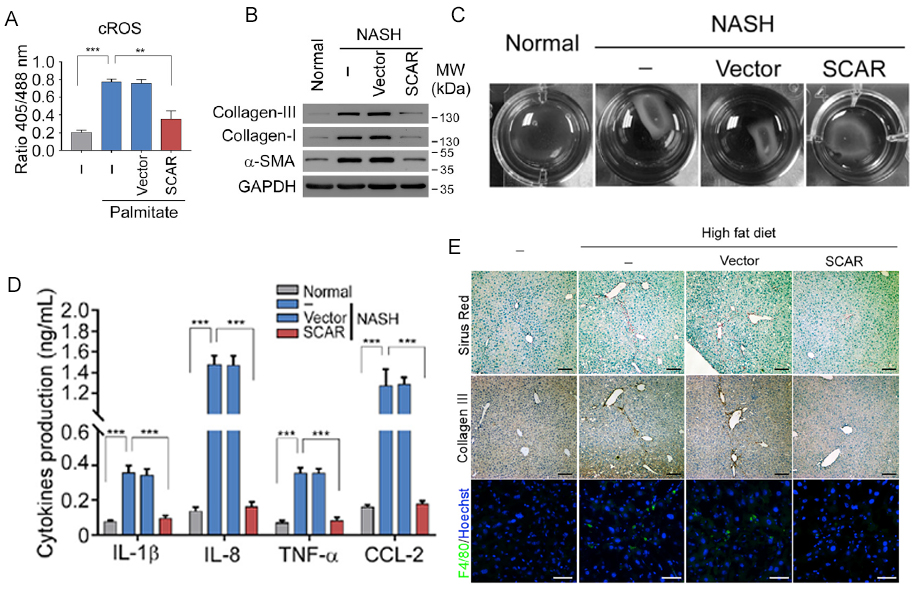
圖2. 過表達SCAR抑制NASH相關表型。
A:正常肝成纖維細胞在使用棕櫚酸酯模擬脂質暴露的情況下,过表达SCAR對於細胞質中ROS(cROS)含量的影響。B:Western blot檢測過表達SCAR對於NASH患者肝成纖維細胞活化的影響。C:过表达SCAR對NASH患者肝成纖維細胞收縮性的影響。D:过表达SCAR後NASH患者肝成纖維細胞釋放的細胞因子總量變化情況。E:在高脂餵養小鼠模型中,过表达SCAR導致肝組織中浸潤的巨噬細胞減少。
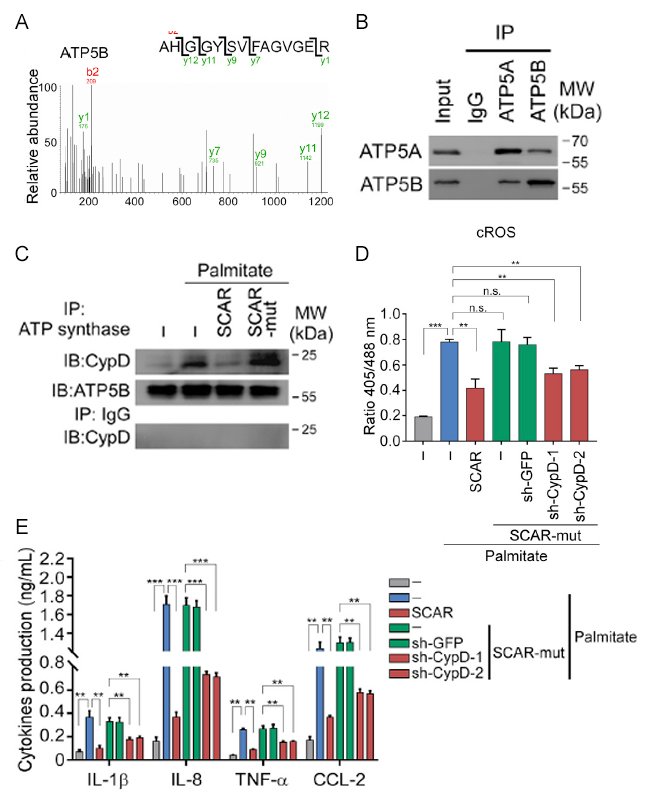
圖3. SCAR發揮功能的下游機制。
A:RNA pull down以及質譜檢測SCAR結合蛋白。B:RIP實驗鑑定ATP5B與SCAR的結合情況。C:SCAR影響CypD與ATP5B的結合。D:SCAR與CypD对于肝成纖維細胞的細胞質中ROS釋放的影響。E:ELISA檢測SCAR與CypD对于肝成纖維細胞釋放細胞因子的影響。
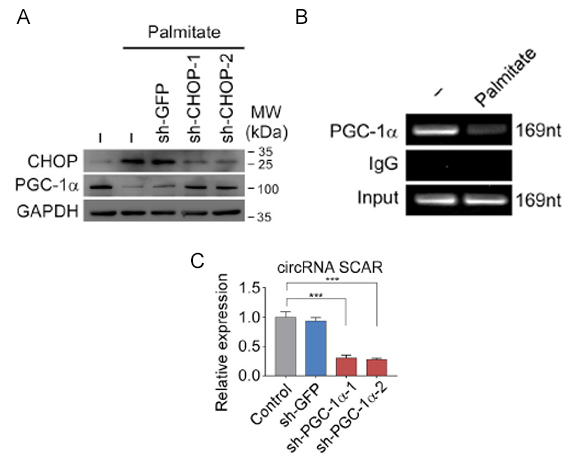
圖4. 調控SCAR表達量的上遊機制。
A:棕榈酸酯模拟脂質暴露的情況下,CHOP表達量上升,PGC-1α表达量下降,敲低CHOP蛋白後PGC-1α表达量降低。B:ChIP實驗分析棕櫚酸酯處理下PGC-1α與SCAR啓動子區結合情況。C:PGC-1α敲低抑制SCAR表達。
研究意義
作者利用Arraystar Human CircRNA芯片在NASH患者肝成纖維細胞中找到了影響NASH發生發展的線粒體定位環狀RNA分子SCAR,在临床样本验证中发现SCAR的表達與人體肝臟健康程度顯著相關。细胞层面上的功能研究表明SCAR與線粒體ROS釋放相關,并且能够抑制肝成纤维细胞的活化以及炎症因子的释放,而小鼠模型上的研究则表明SCAR能夠減輕肝硬化的表型。最后作者通过一系列的机制实验研究发现,在脂质暴露的情况下出现的内质网应激会导致CHOP及其下游PGC-1α的減少,进而导致SCAR的表達量下降。SCAR的減少會導致原本與其結合的ATP5B轉而與CypD結合,从而使线粒体上mPTP通道開放並將ROS釋放到細胞質中最終引起NASH。总体而言,这项工作思路清晰,数据详实,具有很高的科研价值与应用价值,为NASH的治疗提供了新的思路与方法。
文章鏈接
https://linkinghub.elsevier.com/retrieve/pii/S0092-8674(20)31000-X
相關服務

